

Ионообменная смола применяется в водоочистке с 1960-х годов и представляет собой скопление достаточно мелких (меньше миллиметра в диаметре) шариков, изготовленные из специальных полимерных материалов, именуемых для простоты "смолой". Шарики смолы способны улавливать из воды ионы различных веществ и "впитывать" их в себя, отдавая взамен "запасенные" ранее ионы, таким образом, осуществляется ионный обмен.
Ионообменные смолы представляют собой нерастворимые высокомолекулярные соединения с функциональными ионогенными группами, способными вступать в реакции обмена с ионами раствора. Некоторые типы ионитов обладают способностью вступать в реакции комплексообразования, окисления-восстановления, а также способностью к физической сорбции ряда соединений.
Иониты имеют гелевую, макропористую и промежуточную структуру.
Гелевые иониты лишены истинной пористости и способны к ионному обмену только в набухшем состоянии.
Макропористые иониты обладают развитой поверхностью из-за наличия пор и поэтому способны к ионному обмену как в набухшем, так и в не набухшем состоянии.
Гелевые иониты характеризуются большей обменной емкостью, чем макропористые, но уступают им по осмотической стабильности, химической и термической стойкости.
Иониты представлены анионитами и катионитами.
Катиониты представляют собой высокомолекулярные твердые нерастворимые поликислоты, содержащие кислотные группы: сульфогруппы, карбоксильные, фосфиновокислые, селеновокислые и др. Они диссоциируют в воде на малоподвижный макроанион (матрица) и подвижные катионы: RAn- | Kt+.
Катиониты, у которых все подвижные ионы представлены ионами водорода, обозначаются как H-катиониты или H-форма катионита. В тех случаях, когда вместо водорода подвижные ионы представлены катионами металлов (Na+, Ca2+ и др.), применяется соответствующее обозначение солевой формы Na- или Ca-катионит либо Na- или Ca-форма катионита.
Катиониты можно разделить на сильнокислотные и слабокислотные. Сильнокислотные катиониты способны обменивать противоионы на внешние ионы в щелочной, нейтральной и кислой средах. Слабокислотные катиониты обменивают противоионы на другие катионы только в щелочной среде. К сильнокислотным относят катионитам с сильно диссоциированными кислотными группами – сульфокислотными. К слабокислотным относят катиониты со слабо диссоциированными кислотными группами – карбоксильными.
Катиониты подразделяются на:
· сильнокислотные, обменивающие катионы в растворах при любых значениях рН;
· слабокислотные, способные к обмену катионов в щелочных средах при рН > 7.
Синтетические аниониты содержат в макромолекуле функциональные группы основного характера и представляют собой твердые полимерные основания. Аниониты диссоциируют в воде на малоподвижный макрокатиоин (матрица) и подвижные анионы: RKt+ | An-.
Слабоосновные аниониты имеют в своем составе первичные, вторичные, третичные и четвертичные аминогруппы, сильноосновные аниониты содержат четвертичные аминогруппы. Сильноосновные аниониты обменивают противоионы в щелочной, нейтральной и кислой средах, а слабоосновные – только в кислой среде. Как уже отмечалось, аниониты могут поставляться в гидроксильной (OH-) или солевой (Cl-) форме. При длительном хранении анионитов в гидроксильной форме их обменная емкость может снижаться, что, скорее всего, связано с окислением этих полимеров. В результате этого число свободных основных групп уменьшается. Поэтому хранить смолы рекомендуется в солевой форме и в увлажненном состоянии.
Аниониты подразделяются на:
· сильноосновные, способные к обмену анионов любой степени диссоциации в растворах при любых значениях рН;
· слабоосновные, способные к обмену анионов из растворов кислот при рН 1-6;
· промежуточной и смешанной активности.

Также выделяют группу смол под общим названием «амфотерные иониты» или «полиамфолиты». Они содержат подвижные кислотные и основные группы и в зависимости от условий могут проявлять себя как катиониты или аниониты.
Ионит состоит из матрицы (каркаса) – высокомолекулярная, практически нерастворимая в воде или других растворителях часть ионообменного материала, обладающая определенным зарядом (у катионитов – отрицательный, у анионитов – положительный). С матрицей связаны подвижные ионы – противоионы. Противоионы обладают зарядом, противоположным заряду ионогенной группы матрицы. В целом зерно ионообменного материала нейтрально. Противоионы подвижны и способны обмениваться на ионы того же знака. Для наглядности ионит можно сравнить с губкой, в порах которой циркулируют противоионы. Если погрузить губку в раствор, противоионы переместятся в раствор, а их место займут ионы того же знака из раствора, чтобы сохранить электронейтральность зерна.
Если ионит, содержащий только противоионы одного типа, поместить в раствор с противоионами другого типа, то ионы первого типа начнут замещаться на ионы второго типа.
Этот процесс будет продолжаться до тех пор, пока не установится равновесие: ионит и раствор будут содержать ионы двух видов в определенном соотношении. Такое состояние принято называть ионообменным равновесием. Помимо противоионов в ионит поступают растворитель с растворенными в нем ионами – катионами. Катионы – ионы, обладающие тем же зарядом, что и матрица ионита.
Сегодня наиболее применяемыми являются макропористые иониты. Их преимуществами являются малое изменение объема, хорошо адсорбируют, имеют продолжительные обменные реакции, большую скорость фильтрации, прочность и жесткость. Поры в микропористых смолах являются результатом искусственного процесса: добавления жирных кислот, спиртов и гептана.
Если сравнить существующие виды ионитов, то видно:
· макропористые иониты прочнее гелиевых структур;
· гелиевые аниониты работают хуже гелиевых катионитов;
· полистирольные аниониты слабее акриловых.
Важнейшим показателем ионообменных смол является влажность, так как в силу гидрофильности функциональных групп ионообменных смол влага, содержащаяся в смоле, является "химически связанной". Причем специальное удаление этой влаги приведет при последующем использовании смолы только к физическому разрушению гранул. "Внешняя" же влага, не связанная химически с функциональной группой смолы, как правило, удаляется перед упаковкой или с помощью центрофугирования или фильтрования.
Для удобства транспортировки, ионообменные смолы упаковывают по стандартному весу, и продают их определенными объемами - уже для удобства потребителя. Для каждого продукта определяется и постоянно корректируется насыпной вес влажного продукта, основанный на отношении веса к объему (кг/м3).
Следующей важной характеристикой ионообменных смол является ионообменная емкость - весовая, объемная и рабочая.
Весовая и объемная емкости являются стандартными показателями, определяются в лабораторных условиях по стандартным методикам и указываются в паспортных данных на готовую продукцию.
В то же время, рабочая ионообменная емкость не может быть измерена в лабораторных условиях, так как зависит от геометрических размеров слоя смолы и от конкретных характеристик обрабатываемых растворов (уровня регенерации, скорости потоков, концентрации растворенных веществ, требуемых показателей качества обрабатываемого раствора, точного размера частиц).
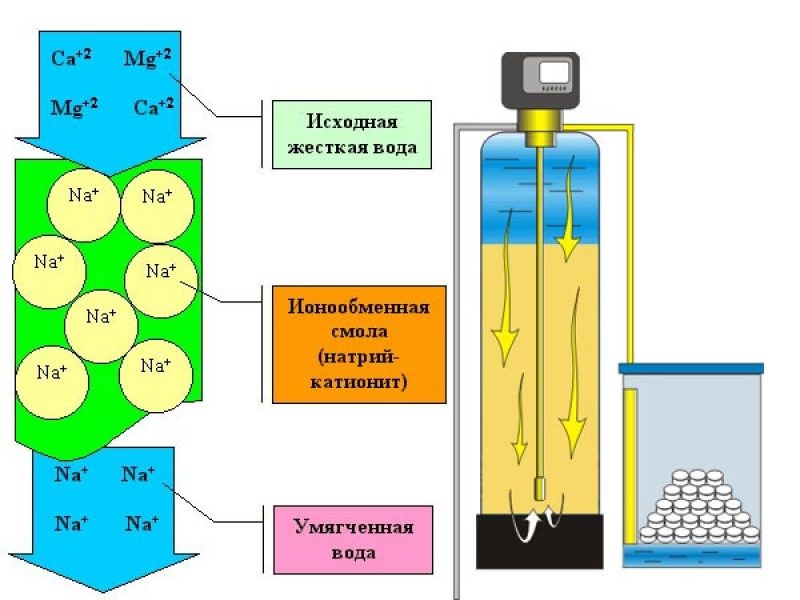
Ионообменные смолы используются в котельных, теплоэлектростанциях, атомных станциях, пищевой промышленности (при производстве сахара, алкогольных, слабоалкогольных и других напитков, пива, бутилированной воды), фармацевтической промышленности и других отраслях.
Ионообменная смола решает только проблему, связанную с повышенной жесткостью воды. Если эффекта умягчения недостаточно, то можно повторно прогнать воду через фильтр, однако при каждой очистке увеличивается концентрация натрия, большое значение которой является опасным для человеческого организма.





